Les biomatériaux sont au centre d’importantes innovations en sciences de la vie. Dans ce secteur où le vieillissement de la population et la croissance du nombre de maladies chroniques sont des enjeux majeurs pour la santé publique, on peut s’attendre à ce que la demande pour des produits médicaux plus performants augmente, d’où la nécessité de procéder à des recherches à la fine pointe de la technologie. Or, les biomatériaux offrent une multitude de possibilités pour répondre à ces enjeux. Comme leur nom l’indique, ils résultent d’une synergie entre plusieurs disciplines, telles que la science des matériaux et la biologie, ainsi qu’un ensemble de nouvelles techniques comme la biomécanique, la biophysique et la biochimie.
Les biomatériaux sont des matériaux d’origine naturelle ou synthétique utilisés dans les dispositifs médicaux destinés à interagir avec les tissus biologiques. Ces derniers correspondent non seulement aux tissus de soutien comme la peau, les os et les dents, mais aussi au sang, qui comporte plusieurs types de cellules (globules rouges, globules blancs) et diverses substances. Les biomatériaux peuvent être faits de métal et d’alliages métalliques (acier inoxydable, titane, etc.), de céramique (alumine, phosphate, etc.), de polymères (fonctionnels ou résorbables) ou de matériaux d’origine naturelle (tissus biologiques, chitine, cellulose, etc.). Les exemples de tels matériaux sont nombreux : valves cardiaques, prothèses orthopédiques, lentilles de contact faites à partir d’hydrogel, implants, etc. Le tableau suivant fournit de nombreux exemples d’applications de cette technologie :
| Domaine médical | Applications |
| Traitement des maladies cardiovasculaires
Chirurgie orthopédique
Ophtalmologie
Autres |
Simulateurs cardiaques, prothèses et endoprothèses vasculaires, cathéters, valves cardiaques, stents
Orthèses, prothèses de hanche, tendons artificiels, matériel de remplacement ou comblement osseux, réparation de fracture, etc.
Implants, lentilles de contact
Biocapteurs, systèmes de libération contrôlée de médicaments, pompes portables et implantables |
Malgré plusieurs avancées notables réalisées ces dernières années, les biomatériaux conventionnels présentent encore de nombreux défis, comme l’intolérance immunitaire, l’infection, la réaction inflammatoire ou l’incompatibilité. C’est pour surmonter ces difficultés et améliorer les résultats des traitements médicaux que les recherches sont entreprises. Elles visent notamment à assurer la sécurité et l’efficacité des biomatériaux dans l’organisme. Puisqu’ils entrent en contact avec le corps humain, ils doivent répondre à l’exigence de la biocompatibilité. Cette dernière fait référence à la capacité du biomatériau à remplir sa fonction avec une réponse appropriée, c’est-à-dire sans effets adverses sur l’environnement biologique avec lequel il entre en contact. Autrement dit, le corps doit accepter les composantes du biomatériau ainsi que ses produits de dégradation. Ainsi, un biomatériau ne doit pas susciter d’effets tels que des réactions inflammatoires, de l’infection ou le rejet (intolérance immunitaire).
Les nouveaux biomatériaux s’illustrent dans des domaines comme l’ingénierie tissulaire ou la médecine régénérative, le diagnostic médical précoce, le traitement cardiovasculaire, la nanochirurgie, la thérapie cellulaire et même la livraison ciblée de médicaments dans les tissus biologiques. Les développements émergents vont des nouveaux hydrogels aux matériaux intelligents avec des cellules souches, en passant par les résines dentaires biodégradables.
Ce bulletin vise à présenter les technologies de pointe en biomatériaux récemment développées ou en cours à Montréal. La première partie est consacrée à la présentation du marché mondial des biomatériaux et des applications biomédicales émergentes. La deuxième partie présente les technologies de pointe développées par les chercheurs et les entreprises montréalaises. Il est à noter qu’il s’agit d’une présentation non exhaustive de toute l’offre technologique montréalaise en biomatériaux. Finalement, une conclusion générale synthétise l’ensemble du contenu et souligne la portée des biomatériaux dans un contexte de changements démographiques. Les définitions de certains termes sont également présentées en annexe.
LE MARCHÉ DES BIOMATÉRIAUX EXPLOSE, DYNAMISANT AINSI CEUX DE L’INGÉNIERIE TISSULAIRE ET DE LA LIVRAISON DE MÉDICAMENTS DANS LE CORPS
- Les biomatériaux
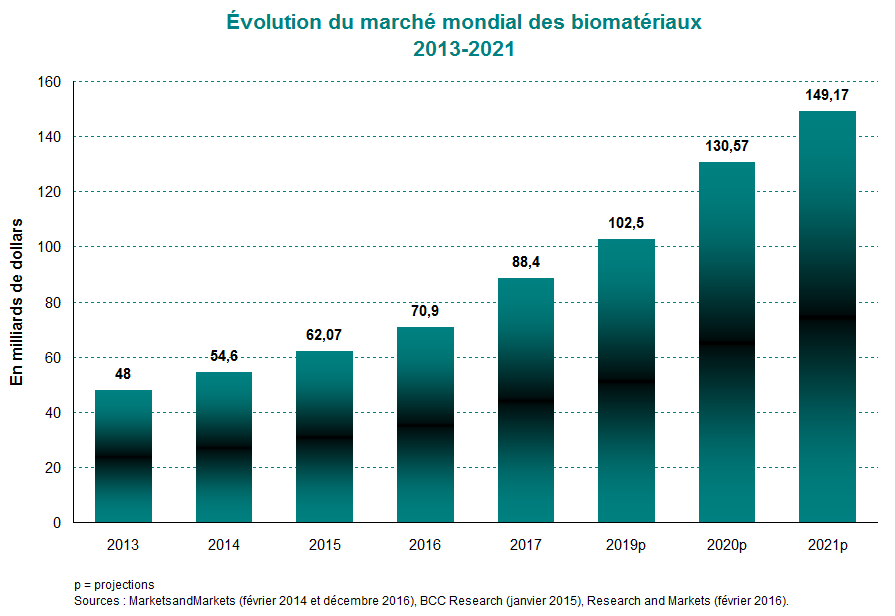
Le marché mondial des biomatériaux était estimé à 62 milliards de dollars en 2015, contre 48 milliards de dollars en 2013. Ce qui représentait une croissance annuelle moyenne d’environ 14 % entre 2013 et 2015. De 2016 à 2021, ce marché devrait croître en moyenne de 16 % par année pour atteindre plus de 149 milliards de dollars en 2021. Le marché nord-américain des biomatériaux représentait à lui seul près de 37 % du marché mondial avec 22,75 milliards de dollars en 2015. Toutefois, cette part devrait légèrement baisser en 2020 et représenter 34 % du marché mondial. La croissance soutenue du marché des biomatériaux bénéficie à plusieurs applications émergentes, comme la livraison ciblée de médicaments et la régénération des tissus humains.
- Les systèmes avancés de livraison de médicaments
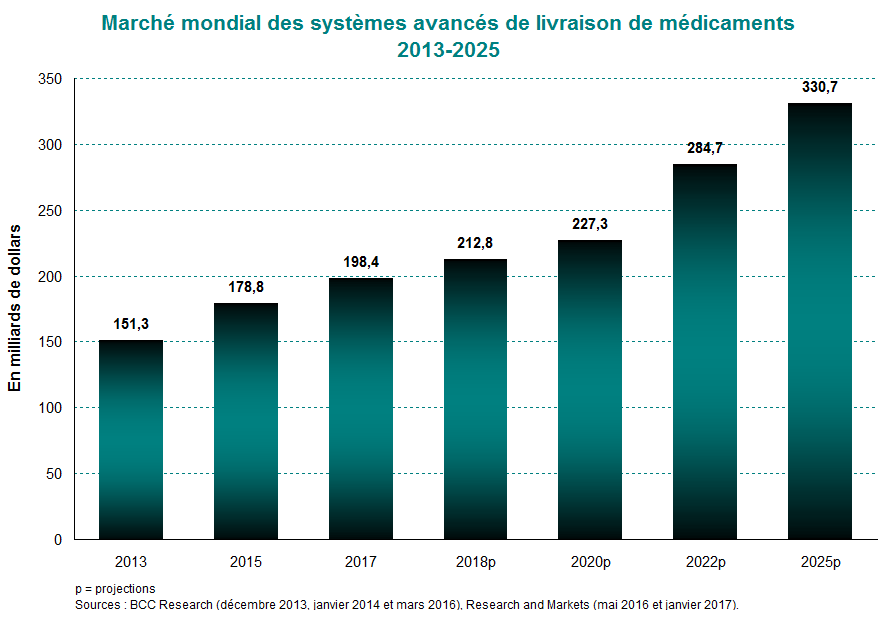
En 2015, le marché mondial des systèmes avancés de livraison de médicaments était estimé à environ 179 milliards de dollars, contre 151 milliards en 2013, enregistrant ainsi un taux de croissance moyen de 9 % par année. Cette industrie devrait maintenir une croissance annuelle moyenne de 6 % au cours des dix prochaines années pour atteindre près de 331 milliards de dollars en 2025. Les marchés nord-américains et européens sont principalement responsables de cette forte croissance. En 2015, ils représentaient à eux seuls 74,4 % des revenus mondiaux. Cette part devrait demeurer élevée au cours des prochaines années, s’élevant à 73 % en 2020.
- L’ingénierie tissulaire et la médecine régénérative
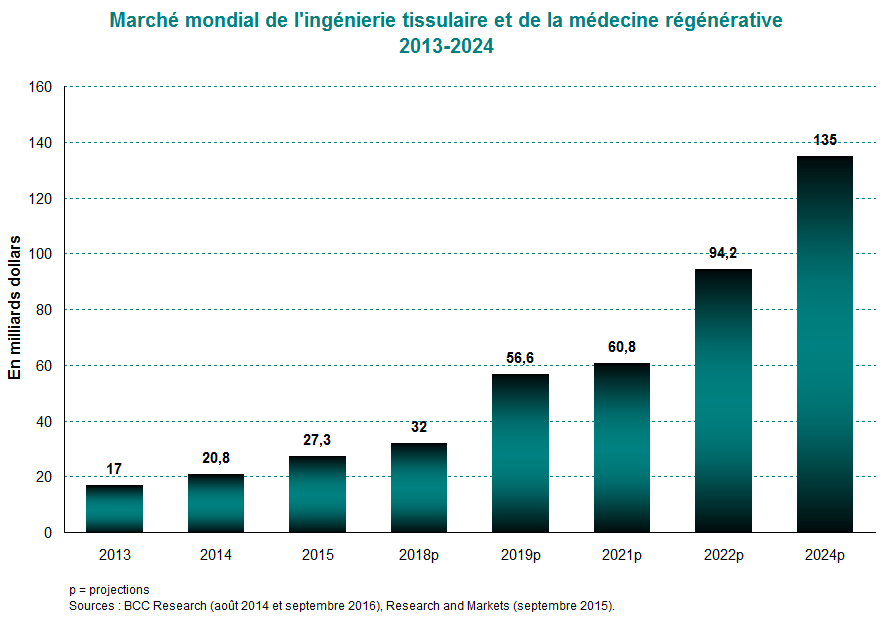
Le marché mondial de l’ingénierie tissulaire et de la médecine régénérative était évalué à 27 milliards de dollars en 2015, enregistrant un taux de croissance annuel moyen de 27 % entre 2013 et 2015. Ce taux de croissance devrait se maintenir entre 2018 et 2024, puisque ce marché passera de 32 milliards de dollars en 2018 à 135 milliards de dollars en 2024. La croissance de cette industrie est stimulée par les marchés nord-américains et européens. À eux seuls, ils représentaient 83 % du marché mondial en 2014. En 2019, cette proportion restera élevée puisque ces économies représenteront 80 % du marché mondial.
Cette industrie se développe principalement dans les économies avancées, en particulier en Amérique du Nord et en Europe. Selon plusieurs analystes, les facteurs comme le vieillissement de la population ou l’augmentation de l’espérance de vie jouent un rôle important dans la croissance du marché des biomatériaux. En outre, les politiques gouvernementales favorables à la réalisation d’essais cliniques et le soutien financier à la recherche contribuent également à stimuler la croissance de ce marché.
MONTRÉAL, UN TERREAU FERTILE AU DÉVELOPPEMENT DES BIOMATÉRIAUX
En raison de leurs propriétés de biocompatibilité et de biodégradabilité, en plus d’être inorganiques, les biomatériaux connaissent un engouement en recherche et développement de pointe. Les entreprises et les chercheurs montréalais s’illustrent tout particulièrement dans des domaines prometteurs, comme le dosage et l’administration ciblée de médicaments, l’amélioration de l’ingénierie tissulaire et les traitements moins invasifs.
- Sophie Lerouge | Hydrogels et revêtements bioactifs pour des thérapies minimalement invasives
Sophie Lerouge, professeure à l’École de technologie supérieure (ÉTS), titulaire de la Chaire de recherche du Canada sur les biomatériaux et implants endovasculaires et chercheuse au Centre de recherche du CHUM de Montréal (CRCHUM), développe des biomatériaux novateurs afin de résoudre des problèmes cliniques variés. Elle cherche notamment à rendre les thérapies moins invasives et plus ciblées, afin de réduire le coût et les complications liées aux traitements chirurgicaux conventionnels.
Ses travaux, menés en étroite collaboration avec des cliniciens et l’industrie biomédicale, s’articulent sur deux axes : la création de nouveaux revêtements et le développement d’hydrogels. La conception de revêtements bioactifs, fabriqués par procédés plasma et greffage chimique de biomolécules, vise la modification de la surface des matériaux pour une optimisation de la réponse biologique du corps humain. Les résultats découlant de cet axe de recherche mènent à une nouvelle génération de dispositifs médicaux, tels que des endoprothèses, des stents métalliques ou des prothèses vasculaires pour le traitement des maladies cardiovasculaires. Ces revêtements bioactifs peuvent s’appliquer aux implants traditionnels et permettent d’améliorer leur efficacité et de réduire les complications, sans altérer pour autant leurs propriétés volumiques et leur durabilité, facilitant ainsi le transfert technologique.
Le développement d’hydrogels injectables, une part importante de ses recherches, vise à développer et à optimiser la thérapie cellulaire et la régénération des tissus biologiques. Conçus pour éviter les effets secondaires et réduire le caractère invasif des interventions chirurgicales, ces hydrogels présentent plusieurs avantages. Tout d’abord, ils sont thermosensibles, c’est-à-dire liquides à basse température et solides à la température du corps humain, ce qui les rend facilement injectables tout en offrant une bonne cohésion mécanique une fois gélifiés. De plus, ils sont biocompatibles et permettent une excellente survie des cellules à l’intérieur du gel.
Grâce à ces hydrogels novateurs, il est possible de libérer localement des molécules ou des cellules de façon ciblée. De plus, ces hydrogels servent de matrice pour la régénération des tissus. Ils sont principalement conçus pour améliorer le traitement des maladies comme le cancer et la dégénérescence des tissus cardiovasculaires et orthopédiques.
À titre d’exemple, la professeure Lerouge a ainsi mis au point un biogel dans lequel les cellules immunitaires du patient peuvent être introduites pour un traitement local du cancer. Conçu à partir de chitosane, issu de poudre de carapace de crustacés, ce biogel est liquide à température ambiante et se gélifie à 37 degrés. Il est donc facilement injectable à l’aide d’une aiguille ou d’un cathéter, et ce, à l’endroit précis où se trouve la tumeur. Les cellules immunitaires y croissent et peuvent sortir du gel pour aller attaquer la tumeur. Ses travaux, effectués en collaboration avec Réjean Lapointe, chercheur à l’Université de Montréal, sont une première percée vers une immunothérapie localisée, qui représenterait un avantage indéniable comparativement aux traitements conventionnels, où les médicaments utilisés sont diffusés dans l’ensemble du corps, ayant ainsi des effets secondaires indésirables, en plus de coûter très cher.
Grâce aux avancées technologiques de sa chaire de recherche, Sophie Lerouge a réussi à établir des contacts pertinents avec l’industrie biomédicale, tant au niveau local, national qu’international.
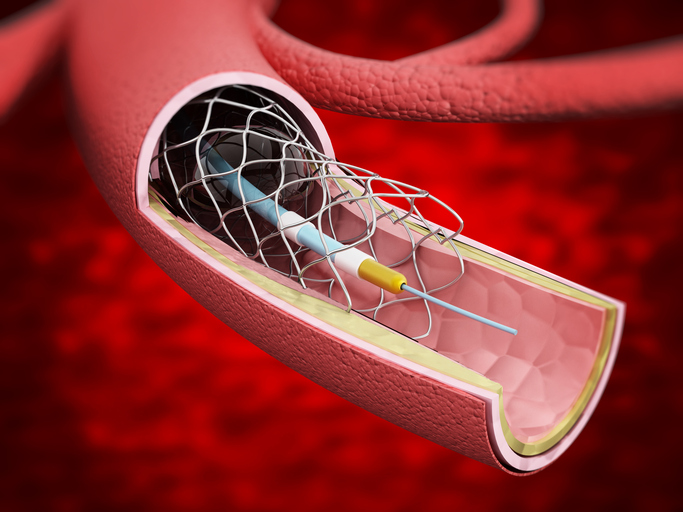
Stent métallique
- Julian Zhu | Biomatériaux à base d’acide biliaire pour des applications biomédicales et pharmaceutiques
Le professeur Julian Zhu, titulaire de la Chaire de recherche de l’Université de Montréal en biomatériaux polymères concentre ses recherches sur le développement des biomatériaux polymères pour des applications biomédicales et pharmaceutiques. Plus précisément, il développe des polymères biodégradables, des résines dentaires novatrices, des hydrogels et même des biocapteurs. Ces biomatériaux sont conçus à base de composés naturels, entre autres d’acides biliaires, une famille de biocomposés qui existent en grande quantité dans le corps et qui ont l’avantage d’être non toxiques et biocompatibles. Ils seraient, selon le chercheur, de bons candidats pour des applications dans le domaine biomédical.
Parmi ses technologies novatrices brevetées, il a développé des résines dentaires qui, contrairement à celles sur le marché, sont biocompatibles, non toxiques et présentent de bonnes propriétés mécaniques. Les résines dentaires conventionnelles utilisent comme produit de départ du bisphénol A (BPA), une substance organique toxique pour la santé et pour l’environnement, dans la préparation de certaines matières plastiques. Le BPA est reconnu comme un perturbateur endocrinien qui cause des problèmes cardiovasculaires et reproductifs, et des cancers. Le développement des résines dentaires à base de substances biocompatibles pour le corps permettrait de prévenir en amont ces risques pour la santé.
Autre avancée prometteuse et brevetée, le chercheur et son équipe sont parvenus à mettre au point des polymères biodégradables. Grâce à l’utilisation d’acides biliaires, ils ont conçu des polyesters biocompatibles dont la vitesse de dégradation peut être contrôlée. Les résultats de cette recherche pourraient mener au développement de plusieurs produits biomédicaux, notamment la fabrication de bandages pour l’ingénierie tissulaire, de stents à polymères biodégradables dont la forme pourra être contrôlée lors des opérations chirurgicales, et même de fils de suture intelligents.
Il a également mis au point des hydrogels novateurs, composés de glucose et d’acides biliaires, qui présentent une bonne biodégradabilité et une diversité fonctionnelle. Les avantages de ces nouveaux matériaux aqueux permettant une autoguérison seraient énormes pour le secteur médical. Ces hydrogels ont la capacité de favoriser une régénération automatique des tissus mous. Ils peuvent, à titre d’exemple, être utilisés pour une autocicatrisation des sutures ou encore pour l’administration ciblée de médicaments.
Les différents biomatériaux présentés ici, qui ne sont qu’un aperçu des résultats des recherches du professeur Zhu, sont à ce jour disponibles pour être commercialisés. Un partenariat avec l’industrie accélèrerait leur commercialisation.
- L’Hocine Yahia | Des nanoparticules superparamagnétiques et des bactériophages pour des applications en nanomédecine
Le développement d’un système de livraison de médicaments à l’échelle nanométrique représente un défi important en raison de la dispersion des nanoparticules dans les cellules biologiques. L’Hocine Yahia, directeur du Laboratoire d’Innovation et d’Analyse de Bioperformance de Polytechnique Montréal et affilié à la Faculté de médecine de l’Université de Montréal, développe des biomatériaux intelligents qui pourraient influencer fortement la réponse cellulaire. Ses deux principaux axes de recherche actuels concernent la conception d’une plate-forme de nanoparticules superparamagnétiques, et la mise au point de méthodes de destruction de bactéries résistantes aux antibiotiques responsables des infections nosocomiales. Ces dernières sont acquises au cours d’un épisode de soins médicaux dans un établissement de santé et touchent autant les patients que les soignants.
Le développement de la plate-forme des nanoparticules superparamagnétiques vise des applications dans le domaine de la nanomédecine. Plus spécifiquement, les recherches entreprises par le professeur Yahia permettront deux principales applications liées au ciblage médical précis dans le corps :
– une injection ciblée de médicaments dans la tumeur;
– une capture spécifique de pathogènes et de protéines dans le sang.
Sous l’action du champ magnétique, les nanoparticules s’échauffent et libèrent de la chaleur (hyperthermie). Conséquemment, au contact d’une tumeur, ces nanoparticules entraînent la destruction des cellules cancéreuses. En outre, les recherches sur cet axe sont entreprises dans l’optique d’augmenter la capacité des matériaux utilisés à réagir à un champ magnétique pour libérer plus de chaleur tout en réduisant la quantité de nanoparticules injectées dans les cellules biologiques. Ces nanoparticules superparamagnétiques permettront d’élaborer de nouvelles méthodes de prévention et de traitement des maladies comme l’athérosclérose, le cancer, le choléra ou la malaria.
L’un des principaux défis liés aux infections nosocomiales est la résistance des bactéries aux antibiotiques développés jusqu’ici pour les prévenir et les contrôler. Les avancées en recherche et développement constituent ainsi une étape importante pour la prise en charge de ce problème. Pour y arriver, les recherches en cours au laboratoire LIAB visent la conception de deux méthodes :
– La première, à base de nanoparticules métalliques, permet de générer des espèces réactives de l’oxygène (en anglais : ROS pour Reactive Oxygen Species);
– La deuxième utilise des virus naturels (ou bactériophages), c’est-à-dire n’infectant que des bactéries. La performance des dispositifs médicaux, tels que les prothèses et les implants, dépend fortement des caractéristiques des biomatériaux utilisés. En particulier, les infections nosocomiales peuvent être transmises à travers ces dispositifs. La méthode proposée par le professeur Yahia et son équipe est d’attacher les bactériophages aux surfaces des implants et des dispositifs médicaux pour empêcher la formation de biofilms microbiens responsables des infections.
À terme, cette recherche mènera au développement de nanodispositifs médicaux pour la prévention et le traitement de maladies, comme le cancer, l’athérosclérose ou les infections nosocomiales qui sont devenues des problèmes de santé majeurs.
- Jung Kwon (John) Oh | Livraison intelligente des nanoassemblages pour le traitement amélioré du cancer
Lors d’une chimiothérapie, on administre une dose de médicaments anticancéreux par voie intraveineuse dans le sang. Idéalement, ces médicaments devraient être administrés à des concentrations thérapeutiques exactes et ciblés sur des tumeurs pour ne tuer que les cellules cancéreuses. Cependant, la livraison de petites molécules de médicaments aux tumeurs n’est souvent pas bien contrôlée, causant des effets secondaires graves ainsi qu’une mauvaise efficacité des médicaments. Ces résultats négatifs sont principalement attribuables à leur petite taille. Ils sont rapidement filtrés par les reins visant leur élimination du sang et la distribution aux tissus normaux.
Dans le but d’améliorer la délivrance de petites thérapies médicamenteuses, des plates-formes à l’échelle nanométrique dont la taille est de 10 à 100 nanomètres ont été développées pour des applications de distribution de cibles tumorales. Une plate-forme prometteuse est le nanoassemblage à base de polymère conçu pour une taille appropriée (50-150 nanomètres de diamètre) qui peut maximiser l’efficacité du médicament et minimiser les effets secondaires indésirables. Les nanoassemblages permettent l’encapsulation de la thérapie anticancéreuse pour qu’elle puisse fonctionner comme les nanothérapies de délivrance de médicaments. Lors de l’injection intraveineuse dans la circulation sanguine, les nanomatériaux chargés de médicaments sont distribués dans le sang. Grâce à un effet de perméabilité et de rétention (en anglais : effet EPR pour Enhanced and Permeability Retention), ils ne visent que les tissus tumoraux et sont ensuite internalisés dans les cellules cancéreuses par endocytose (mécanisme de transport de molécules ou de particules vers l’intérieur de la cellule). En conséquence, les nanomatériaux chargés de médicaments réduisent les effets secondaires indésirables communs aux médicaments anticancéreux et maximisent l’efficacité des traitements.
Toutefois, l’un des défis de ces plates-formes nanométriques demeure, à savoir une distribution stable des médicaments dans les cellules cancéreuses et les tissus tumoraux. Pour s’attaquer au problème, le professeur Oh et son équipe de la Chaire de recherche du Canada en nanobioscience, affiliée à l’Université Concordia, mettent au point une solution novatrice. Celle-ci consiste au design et à la conception de nanomatériaux à base de polymères, capables de se dégrader en réponse à des stimuli, afin d’améliorer la libération ciblée de médicaments à l’aide des nanoassemblages. Ils sont conçus pour être stables sous les conditions physiologiques tout en circulant dans le sang. Cependant, ils sont désassemblés sous une forme contrôlée comme composantes cellulaires pour donner des stimuli appropriés à l’intérieur des cellules tumorales et cancéreuses. Outre le transport efficace de médicaments, ces nouveaux nanomatériaux offrent un grand potentiel à titre d’agent d’imagerie et d’échafaudage de tissus. Pour pousser plus loin leur recherche, le professeur Oh et son équipe ont développé une variété de copolymères à blocs, dégradables et sensibles à des stimuli qui peuvent interagir avec des tissus biologiques. Ils travaillent à une compréhension des fonctions biologiques de ces copolymères à blocs, qui offriraient un énorme potentiel pour le traitement du cancer.
En plus de ces copolymères à blocs, le professeur Oh et son équipe ont développé une variété d’autres nanomatériaux pour des applications biomédicales. Parmi ceux-ci, on retrouve des nanofibres, des polymères thermorésistants et des nanogels. Dans l’ensemble, les recherches entreprises offrent un grand potentiel pour améliorer la qualité de vie des patients atteints de cancer, grâce à des traitements plus efficaces.
- Mircea Alexandru Mateescu | Des applications thérapeutiques à fort potentiel
Les formulations ciblées
L’histamine, un agent allergène et pro-inflammatoire, est commune à de nombreuses pathologies, telles que les allergies et les maladies inflammatoires de l’intestin. À la place des agents antihistaminiques et anti-inflammatoires synthétiques, la diamine oxydase (ou l’histaminase), une enzyme d’origine végétale, pourrait agir sur l’excès d’histamine et ainsi aider à garder la muqueuse intestinale en meilleure santé. Pour rester active et exercer son rôle, l’enzyme doit être formée avec des excipients également non toxiques. Dans ce contexte, l’équipe de Mircea Alexandru Mateescu, professeur au département de chimie de l’UQAM, spécialisé dans le domaine de la biochimie des protéines et des applications pharmaceutiques, propose une solution thérapeutique avec des formulations ciblées à base de biopolymères. Ces derniers confèrent une bonne stabilité au médicament et facilitent la libération de la diamine oxydase au niveau de l’intestin enflammé. À noter que cette enzyme et les excipients de la formulation proviennent de constituants alimentaires non toxiques.
Une autre réalisation prometteuse de l’équipe du professeur Mateescu est le développement et le suivi in vivo de formulations orales ciblant l’immunité mucosale, et ce, en utilisant comme traceur le sulfate de baryum. Ce projet, réalisé par Marc-André Labelle, finissant à la maîtrise en biochimie, vise à proposer une nouvelle méthode de suivi des formulations orales contenant le peptide fimbriae (F4), qui sont destinées à la livraison locale des médicaments dans l’intestin grêle. Pour ce faire, un agent opacifiant nommé le sulfate de baryum (SB) est incorporé dans des comprimés. Il permet de suivre leur trajet et de confirmer la livraison des agents bioactifs à la cible, assurant ainsi leur efficacité. Concernant le suivi in vivo, il sera effectué par rayons X. Selon le jeune chercheur, cette technique est plus perfectionnée que la scintigraphie et moins coûteuse que l’imagerie par résonance magnétique.
La culture cellulaire
Pour soigner les personnes souffrant de certaines maladies chroniques, telles que les maladies du foie (l’hépatite B, C ou D) ou du pancréas, on a souvent recours à la transplantation d’organes ou de tissus. Par exemple, la transplantation hépatique, une intervention chirurgicale permettant de remplacer un foie malade par un foie sain, est nécessaire pour traiter les patients souffrant d’une défaillance de cet organe. Cette option thérapeutique privilégiée est toutefois limitée par certains facteurs, notamment le manque de donneurs. Dans ce contexte, l’équipe du professeur Mateescu fait des recherches afin de trouver des solutions de remplacement à la transplantation d’organes. Celles-ci visent à créer des organes et des tissus à partir des cellules souches. Ils ont conçu des biomatériaux ayant des propriétés mécaniques compatibles, non toxiques et permettant la croissance de tissus tridimensionnels (3D). Concrètement, ils ont développé un nouveau dérivé de l’alcool polyvinylique (en anglais : PVA pour Polyvinyl Alcohol) comme échafaudage pour la culture des hépatocytes dans un microenvironnement 3D. Outre la régénération du tissu hépatique, les échafaudages à hépatocytes peuvent aussi être utilisés pour l’évaluation de divers médicaments et d’agents toxiques.
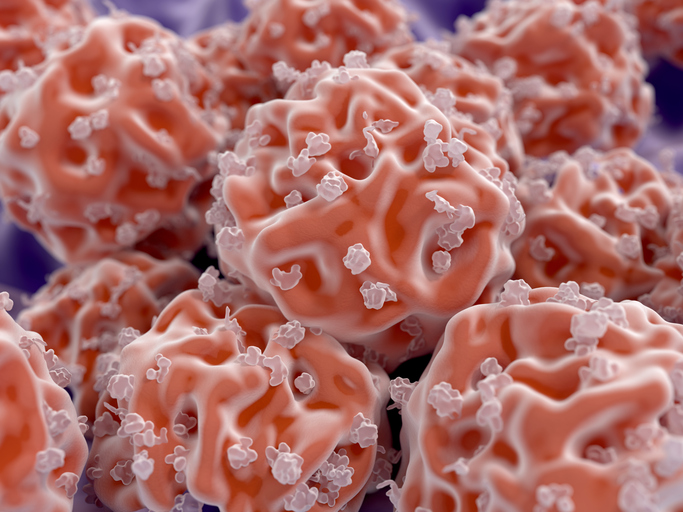
Par ailleurs, toujours dans l’équipe du professeur Mateescu, Nassim Benyerbah, étudiant à la maîtrise en biochimie à l’UQAM, travaille sur le développement d’un matériau tridimensionnel biocompatible et biodégradable, à base de dérivés d’amidon et d’alcool polyvinylique (PVA), pour une utilisation biomédicale telle que la culture cellulaire ou encore les implants. L’objectif est d’obtenir des biomatériaux sous forme d’éponges avec une structure en échafaudage tridimensionnelle. Cette structure est constituée de pores interconnectés, capables d’héberger les cellules et d’offrir des conditions favorables à leur prolifération.

Microscopie électronique à balayage pour des supports à base de PVA-STMP-CMS avec et sans des hépatocytes (48h). Images obtenues à un voltage accéléré de 15 – 30 kV et une magnitude de 100-500 µm. | Crédit image : Prof Mircea Alexandru Mateescu
- Bioastra Technologies | Des matériaux intelligents à la fine pointe de la technologie
L’entreprise montréalaise Bioastra Technologies est spécialisée dans la mise au point de matériaux intelligents et adaptatifs. Grâce à son expertise multidisciplinaire en science des polymères, génie chimique, textiles, science des surfaces et génie biomédical, elle a acquis une position de chef de file mondial dans ce domaine.
L’entreprise développe des polymères intelligents capables de modifier leurs propriétés intrinsèques lorsqu’ils sont soumis à un stimulus externe comme le stress, la température, l’humidité, le pH, les champs électriques, les champs magnétiques, etc. Dotés de propriétés multifonctionnelles, ces matériaux ont une multitude d’applications, entre autres les dispositifs médicaux. Parmi les produits développés par l’équipe de jeunes chercheurs de Bioastra Technologies, on retrouve les matériaux sol‑gel thermosensibles utilisés pour l’embolisation ou le relargage de médicaments. Ces matériaux ont la propriété de passer de la forme liquide (sol pour solution) à une forme solide (gel), une transition accompagnée par des changements physiques. Ces derniers concernent le passage d’un liquide majoritairement visqueux vers un solide majoritairement élastique et aussi structurel (changement de la porosité).
L’équipe de recherche réalise d’autres activités, telles que le développement de capteurs flexibles polymériques ou encore de muscles artificiels à partir de polymères électroactifs. Ce type de polymère se distingue par sa capacité à convertir l’énergie électrique en mouvement et en force, et vice versa.
- Oligo Medic | Une solution novatrice pour les patients souffrant de pertes avancées de cartilage
Les douleurs articulaires sont souvent dues à l’usure du cartilage, un tissu conjonctif sous forme d’interface entre les extrémités osseuses et dont la principale fonction est d’assurer la mobilité et la flexibilité de l’articulation. Contrairement aux os, le cartilage est vulnérable, sa régénération est faible et sa cicatrisation est difficile. Il est souvent confronté à des maladies pouvant causer des lésions tissulaires irréversibles. L’arthrose est un bon exemple de maladie dégénérative qui s’attaque au cartilage des articulations. Touchant principalement les personnes âgées et les jeunes sportifs, elle peut mener à la destruction totale du cartilage et entraîner une douleur intense. Les solutions envisagées jusqu’ici sont la pose de prothèses et la prise de médicaments afin d’atténuer la douleur.
Pour remédier à ce problème, l’entreprise Oligo Medic, spécialisée dans le développement de biomatériaux novateurs, a mis au point un produit innovant et breveté permettant de régénérer le cartilage. Baptisé « JointRep », il s’agit d’un hydrogel à base de polyglucosamine ayant des propriétés thermogélifiantes. Ainsi, il se solidifie rapidement une fois injecté et chauffé à la température du corps. Le produit présente l’avantage de fournir une matrice d’échafaudage biocompatible, isotonique et bioadhésive.
Le dispositif médical est administré de façon percutanée par intervention chirurgicale arthroscopique sous anesthésie locale. Concrètement, une caméra miniature à fibre optique pour visualiser la lésion et un tube permettant d’introduire des outils sont insérés dans le genou. La lésion est polie pour produire une surface lisse et des trous sont ensuite percés afin de libérer les cellules souches de la moelle osseuse. Une fois appliqué sur la lésion et exposé à la température corporelle, l’hydrogel se transforme en gel solide procurant un échafaud à partir duquel les cellules souches produisent un nouveau cartilage sain. Seulement 90 minutes après son opération, le patient obtient ainsi son congé et peut quitter l’hôpital en se déplaçant à l’aide d’une cane. Il pourra également reprendre ses activités régulières après seulement trois semaines.
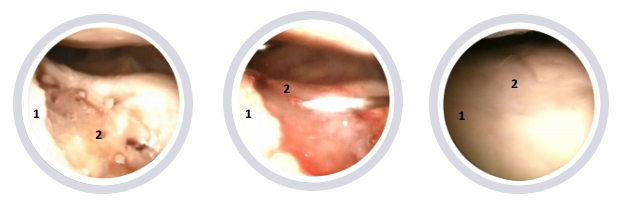
De gauche à droite: défaut dans une fosse inter-condylienne préparée pour JointRep™, défaut rempli avec le matériau, défaut après six mois | Zone 1: Cartilage sain – Zone 2.: défaut | Crédit image : Oligo Medic
Des essais cliniques ont été réalisés en Europe sur des patients âgés de 18 et 75 ans et souffrant de perte avancée de cartilage. Les sujets ont été sélectionnés pour réaliser le traitement de la microfracture ou pour le traitement de la microfracture avec le produit JointRep. Après six mois, les résultats cliniques pour le groupe traité avec l’hydrogel JointRep étaient très concluants. En effet, le produit a permis de réduire la douleur en plus d’augmenter l’habileté physique et la mobilité pour toutes les tranches d’âges.
Le produit JointRep a obtenu le Marquage CE (conformité européenne) pour l’utilisation dans toutes les articulations du corps et il est actuellement commercialisé dans quinze pays à travers le monde, mais il ne l’est pas encore en Amérique du Nord. Des démarches ont été entamées en vue d’obtenir une approbation du Secrétariat américain aux produits alimentaires et pharmaceutiques (Food and Drug Administration – FDA) pour le marché américain.
Il importe de relever les défis liés aux changements démographiques et à l’accroissement des maladies chroniques en misant sur des technologies de plus en plus précises. Quel que soit le domaine médical (chirurgie, ingénierie tissulaire, biotechnologie, etc.), le développement des technologies et leur diffusion applicable dans le système de santé font partie des solutions innovantes toutes désignées.
Les technologies montréalaises présentées ici sont révélatrices du fort potentiel des biomatériaux en sciences de la vie, en plus de s’inscrire dans un contexte favorisant de nouvelles applications biomédicales. En particulier, la médecine régénératrice et la livraison ciblée de médicaments apparaissent comme prometteuses. Ces industries étant en évolution constante, surtout avec l’émergence des nouvelles technologies comme la bio-impression 3D et des matériaux plus performants, on peut s’attendre à ce qu’elles jouent un rôle de plus en plus important au cours des prochaines années. Elles ouvrent en outre la porte à de multiples possibilités pour Montréal, déjà reconnue mondialement comme ville innovante en sciences de la vie, notamment en technologies de la santé et en biopharmaceutique.
Classée septième au monde pour sa concentration d’emplois dans ce secteur névralgique, Montréal possède une masse critique d’entreprises de pointe allant des PME aux entreprises multinationales. Le transfert des technologies présentées ici dans l’industrie de la santé s’avère essentiel à la vitalité et à l’innovation du secteur, tout en favorisant le rayonnement de la métropole.